韩国**疗器械产品注册与批准
韩国**疗器械法规
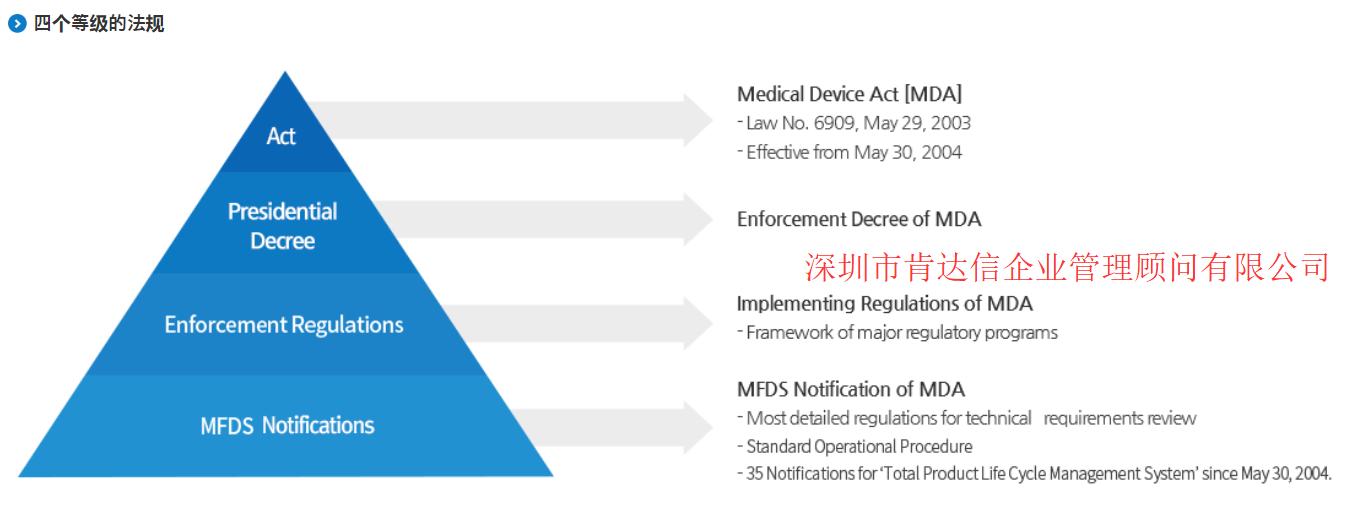
**疗设备受 韩国食品药品安全部(MFDS)的监管,其目的是通过对韩国人民每天所面对的**疗设备进行彻底的安全控制来保护和促进公众健康。**疗设备受《**疗设备法》的约束。
韩国**疗器械注册与批准
**疗器械分为四类,即I,II,III和IV类(I是最低风险,IV是最高风险)。
MFDS对某些设备有特殊的测试要求。通常使用的首选项要求韩国认可的测试实验室进行验证测试。但是,如果测试方法不符合韩国的测试要求,则MFDS不接受国外测试报告。
由韩国MFDS认可的实验室进行的本地类型测试
除文档外,根据设备的风险和类型,可能需要进行特定的临床研究。
MFDS对海外生产基地的审核
除了产品注册,MFDS还控制着本地进口商,分销商以及海外制造基地的质量管理体系。
MFDS要求提交“技术文件”以认证和批准**疗器械。
原则上,I和II类设备由“**疗设备信息和技术支持中心(MDITAC)认证”,“美国**疗设备安全信息研究所(NIDS)和III和IV类设备由MFDS批准”。但是,以下类别中的I类和II类设备必须经过MFDS批准。
>需要临床测试报告的产品
>与数字**疗相关的产品(例如远程**疗系统)
>未定义的名称和分类规
>与药品等结合
1.技术文件
与**疗设备质量有关的文件,例如性能和安全性等。
其中包括有关“预期用途”,“作用机理(MoA)”,“操作(功能)结构”,“原材料”,“使用说明”,“测试规范”等的信息。
2.技术文件分类
技术文件由“申请表”和“补充证据”组成。是否强制提交“临床试验报告”(作为“补充证据”的一部分)决定了应遵循的申请程序。
2.1一般技术文件审查
如果设备与合法销售的设备基本相同,则不需要“临床试验报告”。
2.2安全和有效性审查(SER)
彻底审查了包括“临床口头报告”在内的技术文档
※如果“预期用途”,“作用机理(MoA)”和“原料”等差异会严重影响器械的安全性和有效性,则需要“临床试验报告”
3.上市前批准
一级(通知)
II类(认证,批准)
III,IV级(批准)
**疗器械分类
根据对人类健康的潜在风险分为4类(Ⅰ〜Ⅳ)
与GHTF / IMDRF规则协调一致
根据“**疗设备和按产品分类的产品分类规定”和“体外诊断设备和分类的产品分类规定”,对2109项**疗器械项目进行了确认,但IVDD(体外诊断设备)和225种IVDD项除外。
联系我时,请说是在得易搜分类信息网看到的,谢谢!





 未上传身份证认证
未上传身份证认证  未上传营业执照认证
未上传营业执照认证